
Os antimicrobianos transformaram a medicina moderna ao permitir o tratamento eficaz de infecções que, antigamente, apresentavam alta mortalidade. Entretanto, o uso inadequado desses medicamentos tem favorecido o aumento da resistência bacteriana, representando um problema de saúde pública global. Para alcançar bons resultados terapêuticos e reduzir efeitos adversos, é essencial selecionar o antimicrobiano correto, considerando critérios clínicos e microbiológicos. Este artigo aborda os principais aspectos sobre os antimicrobianos, incluindo conceito, classificação, farmacocinética, farmacodinâmica, critérios de escolha, resistência bacteriana e estratégias para uso racional.
O crescimento da resistência antimicrobiana tem dificultado o controle de infecções previamente tratáveis, exigindo prescrições mais criteriosas e conscientes.
Conceito de antimicrobianos
Antimicrobianos são substâncias capazes de impedir o crescimento ou eliminar microrganismos patogênicos, sendo amplamente empregados no tratamento e na prevenção de infecções. Eles podem atuar sobre diversos agentes infecciosos, incluindo bactérias, vírus, fungos e parasitas.
De forma geral, os antimicrobianos incluem:
-
Antibióticos: produzidos por microrganismos e, eventualmente, modificados em laboratório.
-
Quimioterápicos: sintetizados artificialmente.
Ambos são essenciais para o manejo de infecções e prevenção de complicações clínicas.
Classificação dos antimicrobianos
A classificação pode ser feita de acordo com o efeito sobre os microrganismos, mecanismo de ação, espectro de atividade ou origem.
Quanto ao efeito sobre as bactérias
-
Bactericidas: promovem a morte das bactérias atacando estruturas essenciais, como a parede celular ou o DNA. Exemplos: beta-lactâmicos (penicilinas, cefalosporinas), aminoglicosídeos e fluoroquinolonas.
-
Bacteriostáticos: inibem a multiplicação bacteriana, permitindo que o sistema imunológico elimine o patógeno. Exemplos: macrolídeos, tetraciclinas e sulfonamidas.
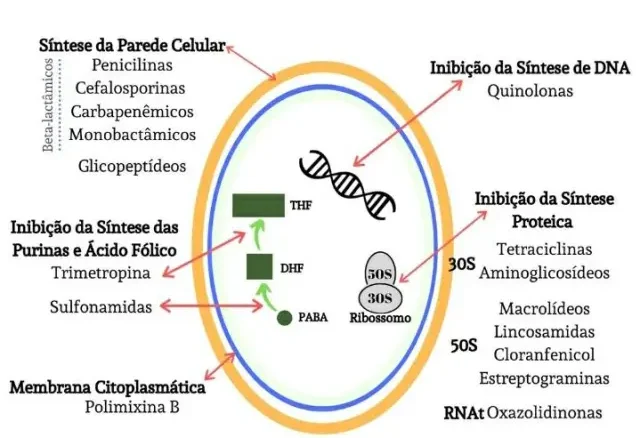
Quanto ao mecanismo de ação
-
Inibidores da síntese da parede celular: impedem a formação da parede bacteriana, tornando as bactérias suscetíveis à lise. Ex.: beta-lactâmicos e glicopeptídeos (vancomicina).
-
Inibidores da síntese proteica: bloqueiam a produção de proteínas essenciais ao crescimento bacteriano. Ex.: aminoglicosídeos, tetraciclinas, macrolídeos, lincosamidas.
-
Inibidores da síntese de ácidos nucleicos: interferem na replicação do DNA ou na transcrição do RNA. Ex.: fluoroquinolonas, rifampicina.
-
Inibidores da síntese de folato: bloqueiam a produção de ácido fólico, necessário para replicação bacteriana. Ex.: sulfonamidas, trimetoprima.
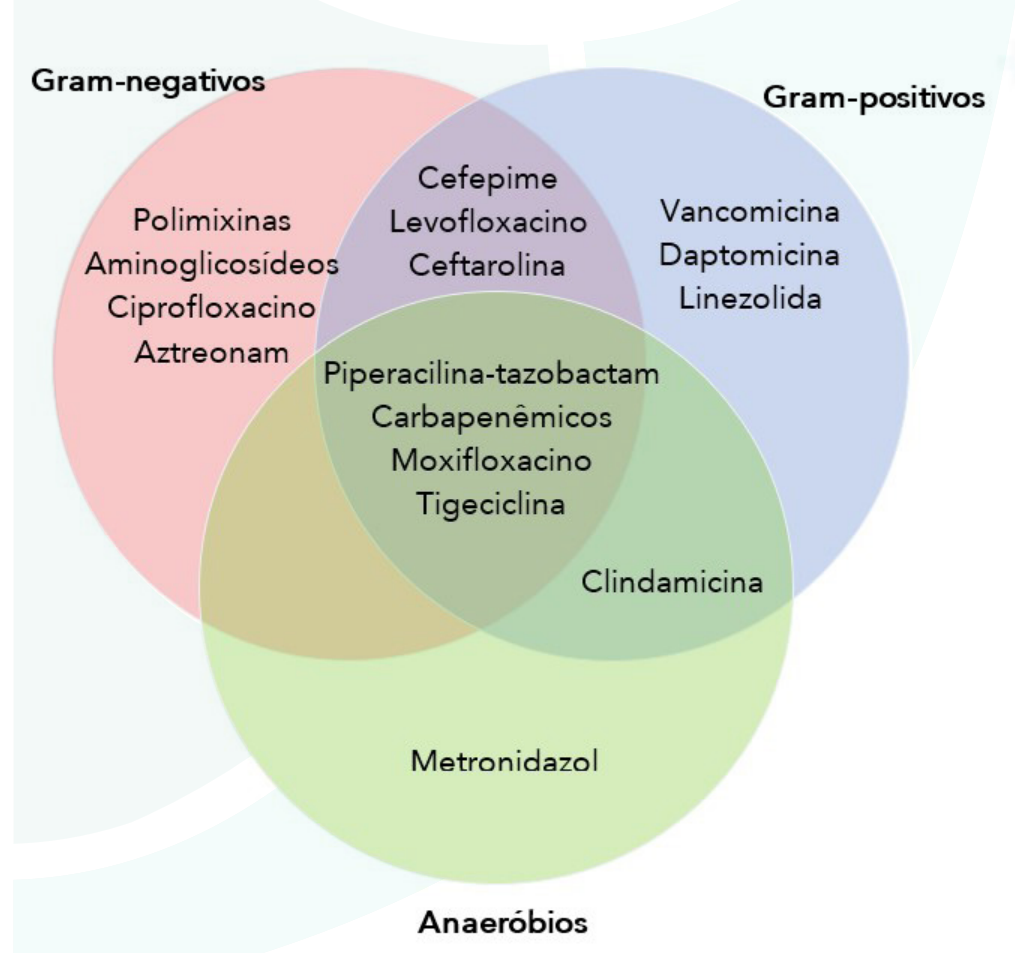
Quanto ao espectro de ação
-
Amplo espectro: atuam contra diversos tipos de bactérias (gram-positivas e gram-negativas). Ex.: cefalosporinas de 3ª geração, carbapenêmicos.
-
Espectro reduzido: agem apenas sobre determinados grupos bacterianos. Ex.: vancomicina (gram-positivas), aztreonam (gram-negativas).
Quanto à origem
-
Naturais: produzidos por microrganismos, como a penicilina.
-
Semissintéticos: derivados de compostos naturais, com modificações químicas para melhorar eficácia e estabilidade. Ex.: amoxicilina.
-
Sintéticos: totalmente desenvolvidos em laboratório. Ex.: sulfonamidas, fluoroquinolonas.
Farmacocinética e farmacodinâmica dos antimicrobianos
A ação dos antimicrobianos depende de fatores relacionados ao fármaco, ao microrganismo e ao paciente. Compreender farmacocinética (PK) e farmacodinâmica (PD) é crucial para uma prescrição adequada.
Farmacocinética
A farmacocinética descreve o caminho do fármaco no organismo:
-
Absorção: ingresso do medicamento na circulação. Exemplos: via oral (fluoroquinolonas, tetraciclinas) e intravenosa (ação imediata). Fatores como alimentos e íons metálicos podem interferir na absorção.
-
Distribuição: dispersão do fármaco nos tecidos. O volume de distribuição (Vd) indica a extensão da penetração. Drogas lipofílicas (rifampicina) penetram tecidos profundos; hidrofílicas (aminoglicosídeos) permanecem no espaço extracelular.
-
Metabolismo: alteração do fármaco no fígado. Penicilinas e cefalosporinas têm metabolismo mínimo; rifampicina é extensamente metabolizada.
-
Eliminação: via renal ou hepática. Aminoglicosídeos e beta-lactâmicos são excretados pelos rins; macrolídeos e tetraciclinas pelo fígado.
Farmacodinâmica
Avalia a relação entre concentração do antimicrobiano e efeito sobre o microrganismo:
-
Dependente da concentração: eficácia maximizada por altas doses (fluoroquinolonas, aminoglicosídeos).
-
Dependente do tempo: eficácia relacionada ao tempo acima da CIM (beta-lactâmicos, macrolídeos).
-
Dependente da AUC/CIM: combina concentração e tempo de exposição (vancomicina).
Critérios para escolha do antimicrobiano
Fatores relacionados ao paciente
-
Idade: recém-nascidos e idosos podem exigir ajustes de dose.
-
Função renal/hepática: insuficiência renal ou hepática altera metabolismo e excreção.
-
Alergias: histórico de reações, principalmente a beta-lactâmicos, deve ser avaliado.
-
Imunidade: pacientes imunossuprimidos podem necessitar de antibióticos bactericidas.
-
Gravidez e lactação: alguns fármacos são teratogênicos (ex.: tetraciclinas).
Fatores relacionados ao microrganismo
-
Agente provável: baseado em sítio da infecção e patógenos mais comuns.
-
Perfil de resistência local: importante para evitar uso de antimicrobianos ineficazes.
-
Teste de sensibilidade: cultura e antibiograma permitem tratamento dirigido.
Fatores relacionados ao medicamento
-
Espectro de ação: amplo espectro para infecções graves; reduzido para patógenos conhecidos.
-
Penetração tecidual: necessária em locais de difícil acesso (ex.: SNC).
-
PK/PD: influência na frequência e dose de administração.
-
Interações medicamentosas: revisão de possíveis efeitos adversos combinados.
-
Toxicidade: aminoglicosídeos podem causar nefro e ototoxicidade.
Resistência bacteriana
Como surge a resistência?
-
Intrínseca: característica natural da bactéria que a torna insensível a certos antibióticos (ex.: vancomicina não atua em gram-negativas).
-
Adquirida: bactéria sensível torna-se resistente por mutações ou aquisição de genes de resistência, transmitidos via transformação, transdução ou conjugação.
Principais mecanismos de resistência
-
Produção de enzimas inativadoras: degradam ou alteram o antibiótico (ex.: beta-lactamases, ESBLs, carbapenemases).
-
Alteração do alvo: mutações reduzem afinidade do fármaco (ex.: macrolídeos e rifampicina).
-
Redução da permeabilidade: diminuição da entrada do antibiótico (ex.: Pseudomonas aeruginosa).
-
Bombas de efluxo: expulsão ativa do fármaco, comum em tetraciclinas e fluoroquinolonas.
